Công nghệ mới nhất cho phép chúng ta tìm kiếm các loại thuốc tiềm năng trong thế giới tự nhiên mà không thu thập hoặc gây hại cho một loài động vật; tất cả những gì bạn cần là ADN của chúng.
Ngày nay, nhiều người trong chúng ta có nhiều khả năng nghĩ về động vật hoang dã với nguồn bệnh của con người hơn là chữa bệnh. Nhưng giống như thực vật, vốn là một phần trong tủ thuốc của chúng ta kể từ khi người Neanderthal sử dụng vỏ cây dương làm thuốc giảm đau, động vật từ lâu đã được khai thác vì tính chất dược liệu của chúng.
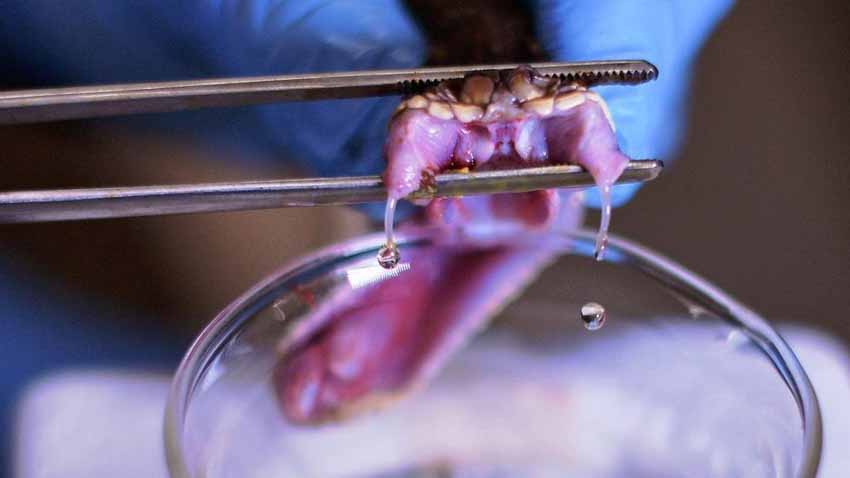
Nọc độc chữa bệnh
Y học cổ truyền Trung Quốc sử dụng các thành phần từ 36 loài động vật bao gồm tê giác, gấu đen, hổ và cá ngựa – nhiều loài trong số đó đang bị đe dọa. Y học Ayurveda khuyến cáo nọc độc của rắn để điều trị viêm khớp, Ayurveda là một hệ thống y học Hindu truyền thống của người Ấn Độ, có niên đại trên 5.000 năm, mang lại nhiều tiềm năng cả theo quan điểm y học phương Đông lẫn y học phương Tây.
Phần lớn các biện pháp truyền thống này không được hỗ trợ bởi bất kỳ bằng chứng khoa học nào – và việc theo đuổi các bộ phận động vật đã góp phần vào một số sự tuyệt chủng, bao gồm tê giác đen phương tây và tê giác trắng phương bắc. Cho đến gần đây, tê tê – nằm trong danh sách một số loài đang bị đe dọa nghiêm trọng – thường được nuôi tại các trang trại động vật hoang dã ở Trung Quốc để lấy vảy.

Trên thực tế, các nhà khoa học hàng đầu đã cảnh báo việc khai thác động vật hoang dã có khả năng dẫn đến những đại dịch thường xuyên và nguy hiểm hơn trong tương lai. Nhưng có thể có một cách để sử dụng động vật hoang dã một cách có trách nhiệm, và đó là nghiên cứu các thành phần hóa học của chúng ở cấp độ phân tử. Nhờ các công nghệ hiện đại, không có thành phần động vật nào được yêu cầu ở bất kỳ giai đoạn nghiên cứu nào – mà chỉ cần một chuỗi ADN.
Không giống như thực vật, từ đó con người đã cô lập các hợp chất cụ thể và biến chúng thành thuốc trong hơn 100 năm, ở động vật, các phân tử cụ thể có tiềm năng y tế trong lịch sử quá khó để xác định hoặc chiết xuất. Nhưng điều đó đang thay đổi, có nghĩa là trong khi nhiều bệnh trong tương lai có khả năng đến từ động vật, một số loại thuốc thú vị nhất của tương lai cũng sẽ đến từ chúng.

Christine Beeton, nhà miễn dịch học Đại học Y Baylor, cho biết: “Chúng tôi đã xem xét thực vật trong một thời gian dài, nhưng rất ít nghiên cứu sâu về động vật”. Beeton nghiên cứu làm thế nào peptide có nguồn gốc từ nọc độc có thể được sử dụng để điều trị các bệnh tự miễn dịch như đa xơ cứng, viêm khớp dạng thấp và loạn dưỡng cơ. Nhờ sự tiến hóa, chúng ta có thể tìm thấy các phân tử lớn gọi là peptide, là anh em ruột của các phân tử tồn tại trong cơ thể con người, cũng như ở các động vật khác.
Điều này có nghĩa là các peptide từ động vật – từ ốc sên và nhện, đến kỳ nhông và rắn – có thể xâm nhập vào các thành phần tế bào của chúng ta như một cây gậy thần, với các hiệu ứng rất chính xác. Các peptide được cấu tạo từ các khối xây dựng tương tự như protein, nhưng trong các chuỗi nhỏ hơn nhiều – người ta có thể nghĩ chúng là các “protein mini”.

Tuy nhiên, vì chúng lớn hơn 10 đến 40 lần so với các loại thuốc phân tử nhỏ như aspirin, peptide đặc biệt hơn nhiều trong những gì chúng nhắm mục tiêu. Kết quả là, chúng ít có khả năng có tác dụng phụ. Ngày nay, các công cụ hiện đại của genomics (khoa nghiên cứu cấu trúc gene), proteomics (bộ môn khoa học nghiên cứu về proteome phát hiện ra những thay đổi trong biểu hiện gen ở mức dịch mã có liên quan đến bệnh) và transcriptomics (những nghiên cứu ở mức độ phiên mã gen) – các nhánh sinh học phân loại cấu trúc hóa học của ADN, protein và các phân tử truyền tin của chúng – đã cách mạng hóa cách các nhà khoa học có thể phát hiện ra các hợp chất trong động vật có khả năng trở thành thuốc chữa bệnh hiệu quả.
Beeton đánh giá: “Bây giờ chúng ta có thể sàng lọc hàng trăm hợp chất trong một tháng. Mười lăm năm trước, điều đó là không thể xảy ra. Bạn sẽ phải nghiên cứu từng hợp chất một, và tiến trình đó phải kéo dài mất 10 năm”. Thay vì phải vất vả lấy nọc từ “milk snake” (một loài rắn bắc Mỹ) và bọ cạp để phân tích, các nhà nghiên cứu chỉ cần khai thác cơ sở dữ liệu mã để tìm peptide với các thuộc tính cụ thể.

Nhiều loại thuốc đã có sẵn trên kệ dược phẩm: Enexatide, có nguồn gốc từ nước bọt của quái vật Gila, được kê toa cho bệnh tiểu đường type 2; Ziconitide, được chiết xuất từ nọc độc của ốc nón (loại ốc vỏ hình nón là tên gọi chung của một nhóm lớn ốc biển có nọc độc) chữa đau mãn tính; Eptifibatide, một mô hình tổng hợp được mô phỏng trên nọc độc của rắn đuôi chuông, được dùng để ngăn ngừa các cơn đau tim; Batroxobin (còn gọi là Reptilase), được chiết xuất từ nọc rắn cực độc pit viper Nam Mỹ và được sử dụng trong một số phương pháp điều trị máu khác nhau; và Captopril, dược phẩm đầu tiên có nguồn gốc từ động vật, một loại thuốc chống tăng huyết áp được Cục quản lý Thực phẩm và Dược phẩm Mỹ (FDA) phê duyệt năm 1981.
Hầu như tất cả các loại dược phẩm có nguồn gốc động vật này đều có nguồn gốc từ nọc độc – một số hỗn hợp hóa học phức tạp nhất được tìm thấy trên trái đất. Mặc dù chúng ta có thể nghĩ nọc độc là những chất độc hiếm mà chỉ một số loài sở hữu, 220.000 loài động vật được biết đến sản xuất những loại cocktail hóa học này.
Chữa bệnh não
Một trong những lĩnh vực hứa hẹn nhất của các loại thuốc có nguồn gốc nọc độc là ngăn ngừa tổn thương não vĩnh viễn do đột quỵ. Mặc dù đây là nguyên nhân gây tử vong đứng hàng thứ hai trên toàn thế giới, giết chết 6 triệu người mỗi năm và để lại thêm 5 triệu người bị tổn thương vĩnh viễn, chúng ta không có phương pháp điều trị nào có thể chữa lành hoặc ngăn ngừa tổn thương não sau khi mất lưu lượng máu đến não. Loại thuốc duy nhất được FDA phê chuẩn cho nhu cầu này là chất kích hoạt plasminogen mô (tPA) được dùng để phá vỡ cục máu đông trong động mạch não. Nhưng chúng ta vẫn chưa có phương pháp điều trị nào có thể ngăn ngừa tổn thương tế bào thần kinh do thiếu oxy.

“Đây là vấn đề lớn nhất mà chúng ta gặp phải: hàng triệu người bị bỏ mặc cho những gì đột quỵ gây cho não của họ trong vài giờ hoặc vài ngày sau đó” – theo Glenn King, nhà hóa sinh Đại học Queensland. King chuyên về các rối loạn hệ thần kinh, trong đó nguyên nhân cơ bản là do khiếm khuyết trong các kênh ion của tế bào thần kinh – các đường hầm nhỏ thông qua các màng cho phép các ion tích điện, giống như sodium (Na), chảy vào và ra khỏi tế bào, kích hoạt các dây thần kinh.
Những khiếm khuyết này có thể xảy ra thông qua sự bất thường về cấu trúc, hoặc số lượng kênh bất thường. Nọc độc chủ yếu nhắm vào các kênh ion. King làm việc với bộ sưu tập mẫu nọc độc lớn nhất thế giới được lấy từ các động vật không xương sống, với peptide được chiết xuất từ hơn 700 loài – bao gồm bọ cạp, nhện, bọ sát thủ và rết. Các độc tố từ côn trùng sẽ tiến hóa trong khoảng thời gian dài hơn nhiều so với động vật có xương sống – trong một số trường hợp 400 triệu năm trở lên.

Khi tìm kiếm nọc độc không xương sống trong “thư viện”của mình, King chỉ tìm thấy một phân tử có vẻ là một ứng cử viên đầy triển vọng để điều trị đột quỵ. Đây là Hi1a, một thành phần của nọc độc từ loài nhện lưới phễu ở Australia gọi là Hadronyche infensa – hỗn hợp gồm 3.000 phân tử mà giáo sư King mô tả là “kho vũ khí hóa học phức tạp nhất trên thế giới”.
Nhện lưới phễu Australia thường là thứ mà chúng ta muốn hoàn toàn tránh xa nhưng loài trông có vẻ sởn gai ốc này có thể sớm giúp ích cho những nạn nhân đột quỵ. Một chuỗi peptide được tìm thấy trong nọc độc của loài này vừa cho thấy giảm tổn hại não vốn xuất hiện trong nhiều giờ sau một cơn đột quỵ với các nghiên cứu tiền lâm sàng trên chuột cho kết quả cực kỳ hứa hẹn.
Trong bài viết năm 2017 trong Kỷ yếu của Viện Hàn lâm Khoa học Quốc gia Mỹ (PNAS), King mô tả các thuộc tính bảo vệ thần kinh của Hi1a ở chuột đột quỵ. Nếu được xử lý vào 8 giờ sau một cơn đột quỵ, Hi1a có thể ngăn chặn “một tổn thương khổng lồ”. Và nếu được xử lý trong vòng bốn giờ, 90% thiệt hại có thể được ngăn chặn, ngay cả với liều lượng cực kỳ nhỏ. Tác dụng phụ với các độc tố này sẽ rất ít hoặc không tồn tại.

King cho biết: “Chất độc không hẳn là nguy hại đối với chúng ta – có hơn 100.000 loài nhện, nhưng chỉ một số ít trong số chúng là nguy hiểm đối với con người”. Ví dụ, thuốc giảm đau Ziconitide, có nguồn gốc từ nọc độc của ốc nón, gây chết cho cá. Nhưng nó chỉ đơn giản là hoạt động như một loại thuốc giảm đau khi được sử dụng cho con người. Làm việc với các kênh ion cũng cho thấy nhiều hứa hẹn trong việc giảm bớt một vấn đề thần kinh phổ biến khác: động kinh. Công trình của King với peptide Hm1a, có nguồn gốc từ nọc độc của loài nhện, cho thấy hứa hẹn cho việc điều trị tình trạng động kinh nghiêm trọng được gọi là hội chứng Dravet.
Dạng động kinh này có tỷ lệ tử vong đột ngột bất ngờ cao gấp 30 lần so với các dạng động kinh khác. Nó cũng rất khó điều trị: các loại thuốc thường được kê đơn như Carbamezapine thực sự có thể làm tình trạng tồi tệ hơn. Trong một bài báo năm 2018, King báo cáo rằng những con chuột được thiết kế có sự thiếu hụt di truyền giống như những người mắc Hội chứng Dravet được phục hồi với một liều nọc độc có nguồn gốc từ loài nhện – và tỷ lệ tử vong của chúng giảm đáng kể.
Hy vọng cho bệnh nhân ung thư
Hiện tại trong các thử nghiệm lâm sàng ở Mỹ và có khả năng được FDA chấp thuận trong vòng 2 năm là Tozuleristide (BLZ-100), một loại “sơn khối u” có nguồn gốc từ nọc độc bọ cạp. Ban đầu được phát triển tại Trung tâm nghiên cứu ung thư Fred Hutchinson ở Seattle và được mô tả trên tạp chí Cancer Research năm 2007.
Hợp chất này liên kết tự nhiên với các tế bào ung thư não và các nhà nghiên cứu đã bổ sung một chất nhuộm huỳnh quang để dưới ánh sáng cận hồng ngoại các tế bào khối u sẽ trở nên dễ dàng phân biệt với mô bình thường. Điều này cho phép các bác sĩ phẫu thuật não dễ dàng nhìn thấy mô ung thư hơn trong quá trình phẫu thuật.

Năm 2004, bác sĩ khoa ung thư Jim Olson của Fred Hutchinson chứng kiến một cô gái tuổi thiếu niên trải qua một cuộc phẫu thuật kéo dài 14 giờ để loại bỏ một khối u não trong đó các bác sĩ phẫu thuật vô tình để lại một mảnh ung thư cỡ ngón tay cái do nhầm nó là mô lành. Quyết tâm không bao giờ để điều gì đó xảy ra lần nữa, Olson giao nhiệm vụ cho các nhà nghiên cứu của mình tìm ra một phân tử cho phép các bác sĩ phẫu thuật nhìn thấy ung thư bằng mắt thường.
Chỉ mất 6 tuần truy quét cơ sở dữ liệu DNA để tìm ra một ứng cử viên phù hợp: Chlorotoxin Cy5.5, có nguồn gốc từ một loài bọ cạp gọi là Leiurus quinquestriatus có nọc độc mạnh thuộc họ Buthidae. L. quinquestriatus có thể được tìm thấy trong sa mạc và môi trường sống cây bụi, từ Bắc Phi qua Trung Đông. Loài bọ cạp này được các nhà nghiên cứu khác ở Alabama phát hiện vào năm 1998 có thể liên kết các kênh ion trên bề mặt của các tế bào khối u não.
Độc tố này cho phép các nhà nghiên cứu nhìn thấy rõ những khối u ung thư. Các nhóm nhà khoa học khác đang nghiên cứu cách sử dụng Tozuleristide để dán nhãn cho các dạng ung thư khác, bao gồm ung thư vú và cột sống. Trong khi đó, một số nhà nghiên cứu đang xem xét các hợp chất có nguồn gốc động vật có thể tiêu diệt ung thư, mà không chỉ “gắn thẻ” nó.

Maria Ikonomopoulou, nhà nghiên cứu Viện nghiên cứu y tế QIMR Berghofer ở Australia, sử dụng Cơ sở dữ liệu ArachnoServer và phát hiện gomesin peptide, có nguồn gốc từ nọc độc của loài nhện đen tarantula tên gọi “Acanthoscurria gomesiana” của Brazil có thể giết chết các tế bào ung thư da. Lấy cảm hứng từ điều này, bà cũng phát hiện ra rằng nọc độc của loài nhện phễu Australia tên gọi H. infensa (cùng loài được King sử dụng trong chữa đột quỵ) có thể tiêu diệt tế bào da ung thư mà không hề gây tổn hại cho các tế bào khỏe mạnh.
Xuất bản công trình trên tạp chí Nature Scientific Reports năm 2018, Maria Ikonomopoulou mô tả cách mà nó có thể được sử dụng để điều trị ung thư tế bào hắc tố (melanoma) – một dạng ung thư da phổ biến thứ 5 ở Anh và ảnh hưởng toàn cầu đến 132.000 người mỗi năm. Ikonomopoulou cho biết: “Các loại thuốc có nguồn gốc từ nọc độc của động vật chủ yếu đến từ rắn vì chúng tạo ra một lượng nọc độc khổng lồ – nhưng bây giờ với cơ sở dữ liệu khổng lồ có được, chúng ta có thể chiết xuất nọc độc từ những động vật không sản xuất với số lượng lớn trong các vết chích của chúng”.
Một con nhện chỉ có thể tạo ra 10ml nọc độc trong một ngày, một con bọ cạp chỉ 2ml – và pseudoscorpion (loài nhện nhỏ có móng vuốt giống bọ cạp) có lẽ ít hơn năm nanolitre (một phần triệu mililittre) mỗi ngày. Nhưng với dữ liệu từ cơ sở dữ liệu mới, các nhà nghiên cứu có thể tổng hợp hóa học các phân tử với các thuộc tính cụ thể với số lượng đủ.
Các peptide chữa chứng đau
Các peptide động vật cũng cho thấy hứa hẹn to lớn trong điều trị chứng đau nơi con người. Chứng đau liên quan đến một loạt các bệnh lý – từ ung thư đến biến chứng đau dây thần kinh do tiểu đường và chấn thương cơ thể thuần túy. Nọc độc là một mỏ vàng cho các phương pháp điều trị tiềm năng, bởi vì những chất độc này đã được “cải tiến” qua hàng triệu năm tiến hóa để nhắm vào hệ thần kinh làm bất động các động vật khác.
Irina Vetter, phó giáo sư Trung tâm Nghiên cứu chứng Đau Viện khoa học sinh học phân tử (IMB) thuộc Đại học Queensland (Australia), cho biết: “Tự nhiên ban cho chúng ta mọi hợp chất hóa học kỳ diệu và chúng ta chỉ có nhiệm vụ nỗ lực hết mình để hiểu biết chúng thấu đáo hơn”. Peptide từ nọc độc sở hữu những đặc tính đáng ngạc nhiên, bất thường và cực kỳ hữu ích. Ví dụ như thuốc giảm đau Ziconitide cho thấy một lợi thế rất lớn so với thuốc phiện ngày nay.
Peptide động vật cũng cho thấy tiềm năng trong điều trị 80 bệnh tự miễn dịch, bệnh đa xơ cứng, viêm khớp dạng thấp vẩy nến, lupus và tiểu đường. Ray Norton, giáo sư Đại học Monash (Australia), bình luận: “Có đến hàng ngàn peptide để lựa chọn – ngày xưa chúng ta sẽ phải nghiền nát một số sinh vật, cô lập một vài peptide khỏi chúng và thử nghiệm để chống lại các bệnh lý khác nhau, nhưng bây giờ chúng ta không còn phải làm điều đó nữa.

Chúng ta có tất cả các chuỗi peptide trong cơ sở dữ liệu. Thử thách bây giờ là biết phải làm gì”. Mande Holford, phó giáo sư hóa học Đại học Hunter ở thành phố New York của Mỹ, người nghiên cứu cách nọc độc có thể được sử dụng để khám phá các loại thuốc giảm đau và ung thư, nói rằng chúng ta không chỉ tìm ra các loại thuốc mới mà nghiên cứu sâu về nọc độc cũng mang đến cơ hội trả lời những câu hỏi lớn về sự phát triển mang lại lợi ích cho nhân loại.
Zachary Crook, nhà khoa học protein lãnh đạo Phòng thí nghiệm Jim Olson tại Trung tâm Nghiên cứu Ung thư Fred Hutchinson ở Washington (Mỹ), đã bắt đầu tìm kiếm cơ sở dữ liệu về các peptide từ một loạt các động vật để tìm kiếm các peptide có thể liên kết với “protein gai” đặc trưng trên bề mặt của virus, hoặc với thụ thể ACE-2 trên các tế bào người mà virus bám vào, để ngăn chặn nó phát huy tác dụng. Crook cho biết: “Mục tiêu cuối cùng của chúng tôi là một loại thuốc được sử dụng bằng cách thuốc hít từ ống hít hoặc máy phun sương để ngăn chặn sự lây nhiễm virus”.
Mặc dù có nhiều ứng dụng từ peptide động vật, tuy nhiên thời gian để tìm giải pháp mới có thể có giới hạn. Do cuộc khủng hoảng đa dạng sinh học mà hàng năm có đến hàng ngàn loài bị tuyệt chủng – thường là trước khi chúng ta phát hiện ra chúng hoặc có cơ hội giải mã bộ gene của chúng. Holford nói: “Chúng ta sẽ mất rất nhiều loài – 10 năm tới rất quan trọng đối với chúng ta để ngăn chặn và cố gắng khôi phục, bảo vệ và học hỏi từ sự đa dạng sinh học mà chúng ta có trên hành tinh này”. Bây giờ, như mọi khi, thiên nhiên có thể cung cấp cho chúng ta cả phương pháp chữa bệnh cũng như tai họa.